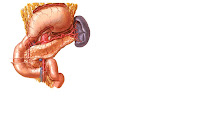
El páncreas es un órgano retroperitoneal. Se relaciona con el duodeno, estómago, bazo, colon, riñón izquierdo, raíz del mesocolon, cava y aorta, tronco celíaco y sus ramas, vasos mesentéricos superiores, vena porta y con el colédoco el cual presenta una porción intra-pancreática.
Irrigación:
Arteria Gastroduodenal.
AMS.
Arteria Esplénica.
Drenaje:
Vena Porta.
VMS.
Vena Esplénica.
FISIOLOGÍA
a) Función exocrina:
- Secreción de enzimas digestivas por células acinares.
- Secreción de agua y electrolitos por células centro- acinares y ductales.
b) Función endocrina: (Islotes de Largenhans).
- Las células alfa secretan glucagon.
- Las células beta secretan insulina.
- Las células “F” secretan polipéptido pancreático.
- Las células delta secretan somatostatina.
Las enzimas digestivas se secretan en forma de zimógenos que luego se activan en enzimas proteolíticas (tripsina y quimiotripsina), glucolíticas (amilasa pancreática) y lipolíticas (lipasas.)
La secreción de sodio y potasio es constante y se corresponde a los niveles plasmáticos de estos electrolitos.
La secreción de bicarbonato es estimulada por la secretina.
El glucagon se contrapone a la insulina.
El péptido pancreático disminuye la secreción pancreática exocrina. También actúa como hormona glucorreguladora.
La somatostatina reduce la secreción exocrina pancreática, disminuye la secreción ácida gástrica y de pepsina, inhibe la actividad motora gastrointestinal, disminuye el flujo sanguíneo esplácnico e inhibe la secreción de Gastrina, secretina, VIP, polipéptido pancreático, insulina y glucagon.
Regulación de la secreción exocrina:
a) Estimulan la secreción de enzimas pancreáticas:
- Acetil-colina por vía vagal desde la fase cefálica de la digestión.
- Gastrina en la fase gástrica.
- CCK en la fase intestinal.
b) Estimula la secreción de bicarbonato:
- La secretina cuya secreción por la mucosa duodenal es estimulada a su vez por la acidificación del medio.
PANCREATITIS AGUDA
Concepto:
Inflamación aguda del páncreas por auto-digestión enzimática del mismo caracterizada por cambios orgánicos y funcionales siempre reversibles (en el tejido pancreático sobreviviente) con afectación regional y sistémica variable.
Se presenta con igual frecuencia en hombres y mujeres.
La pancreatitis ocurre por activación precoz de las enzimas pancreáticas de manera tal que el páncreas se ve afectado por su acción lítica desencadenando fenómenos locales y sistémicos: Síndrome de respuesta inflamatoria sistémica.
Etiología (90%):
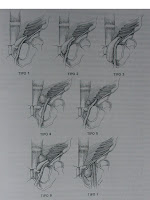
1- Enfermedad litiásica del tracto biliar.
- La migración del cálculo, no necesariamente su impactación desencadenan la pancreatitis.
- Un ducto final compartido entre el Colédoco y el Wirsung está presente en un 90% de los pacientes con historia de pancreatitis biliar.
2- Alcohol.
- Estimula la secreción ácida gástrica y aumenta la resistencia del esfínter de Oddi.
- Aumenta la permeabilidad de los ductos pancreáticos lo que favorece la extravasación de enzimas.
- Produce hipertrigliceridemia.
- El acetaldehído produce lesión pancreática directa.
El alcohol al aumentar la secreción ácida gástrica, aumenta la acidificación del duodeno lo que estimula a su vez la secreción de Secretina la cual estimula la secreción pancreática.
La hiperlipidemia produce lesión endotelial.
La lesión directa del acetaldehído al páncreas se ha demostrado en modelos caninos. Este compuesto es el primer producto estable en la oxidación del etanol.
Etiología (10%):
- Hipertrigliceridemia.
- Hipercalcemia.
- Pancreatitis Familiar.
- Trauma Pancreático.
- Isquemia Pancreática.
- Obstrucción del Ducto Pancreático.
- Obstrucción Duodenal.
- Infecciones Virales.
- Veneno del Escorpión.
- Drogas.
- Idiopáticas.
Hipertrigliciridemia: Sd. Nefrótico, castración, estrógenos exógenos, hiperlipidemias hereditarias.
Hipercalcemia: Hiperparatiroidismo. Dos mecanismos: La precipitación del calcio en los ductos pancreáticos y la activación calcio-inducida del tripsinógeno.
Familiar: Predisposición genética. Historia familiar.
Trauma pancreático: Contuso y penetrante, quirúrgico, CPRE.
Isquemia pancreática: Hipotensión, by - pass cardiopulmonar, Ateroembolismo, Vasculitis.
Obstrucción del ducto pancreático: Tumor, Páncreas Divisum, Estenosis ampular, Infestación por áscaris.
Obstrucción duodenal: Tumores primarios o metastásicos.
Infecciones virales: Virus de la parotiditis, HIV, CMV, Coxsachie B.
Idiopáticas: En un estudio realizado se demostró la presencia de microlitiasis y barro biliar en un 60% de las pancreatitis catalogadas como idiopáticas. En un 40% se debe a pacreatitis autoinmune, también llamada, pancreatitis crónica esclerosante, presenta marcadores inmunológicos positivos, se asocia a otros desordenes inmunológicos como lo son enfermedades del colágeno. Produce esclerosis del páncreas con obstrucción de la vía biliar y del conducto pancreático.
Pancreatitis atópica, cursa con niveles elevados de Ig E.
Drogas Con Asociación Definida
Azatioprina.
Estrógenos.
Drogas Con Asociación Probable
Tiazidas.
Furosemida.
Sulfonamidas.
Tetraciclina.
Corticoesteroides.
Ácido Valpróico.
Clonidina.
Pentamidina.
Procainamida.
Presentación Clínica
- Dolor. Es el síntoma capital y se presenta en un 90% de los casos. Se inicia en epigastrio y se irradia en banda a ambos hipocondrios y espalda. Es continuo y progresa en intensidad.
- Náuseas y vómitos.
- Distensión abdominal por íleo paralítico.
- Signo de Cullen y signo de Grey-Turner.
- Ictericia.
- Compromiso sistémico variable. (Taquicardia, taquipnea, fiebre).
En el caso de la pancreatitis OH¯ el dolor se inicia de 12 a 48 horas posterior a una ingesta copiosa de alcohol. En la pancreatitis biliar el dolor se inicia después de una ingesta de comida rica en granos o grasas.
Signo de Cullen: Equimosis en región periumbilical. Pancreatitis hemorrágica.
Signo de Grey-Turner: Equimosis en flanco izquierdo. Pancreatitis hemorrágica.
Ictericia: en el caso de coexistir con Sd. Ictérico-obstructivo.
Compromiso sistémico variable: Hipotensión, hipovolemia, hipoperfusión, efusión pleural, disnea, cianosis.
Diagnóstico
1- Pruebas De Laboratorio
- Amilasa sérica.
- Iso-enzimas de la amilasa sérica.
- Amilasa urinaria.
- Relación entre el clearance de Creatinina-Amilasa.
- Lipasa sérica.
- Análisis de líquido peritoneal.
2- Examenes Imagenológicos
- Radiografía de tórax.
- Radiografía abdominal.
- Ultrasonido abdominal.
- TC abdominal.
- Resonancia Magnética.
Amilasa: Su aumento se observa después de las primeras 24 horas de iniciados los síntomas con un retorno a la normalidad en los siete días siguientes. Su persistente elevación habla de necrosis, absceso o pseudoquiste. La magnitud de su elevación no habla de la severidad del cuadro. No es específica. Un 10% de las pancreatitis cursan con amilasa normal. Esto se explica porque se está atajando el cuadro ya en resolución, que se trate de una glándula enferma e insuficiente por patología crónica o que se trate de un cuadro grave de necrosis pancreática extensa.
Isoenzima P: Páncreas.
Isoenzima S: Glándulas salivales, Trompas de Falopio, ovarios, endometrio, próstata, mamas, pulmones y probablemente hígado.
Amilasa en orina: Su aumento es más prolongado en el tiempo al compararla con la amilasa sérica.
Relación entre el clearence de Creatinina-Amilasa: 1-4%. Más de un 6% es patológico. No es específico. Amilasa urinaria/amilasa Sérica X Creatinina Sérica/Creatinina urinaria X 100 = tasa de eliminación Amilasa-Creatinina.
Lipasa Sérica: Es mas específica y su aumento es más prolongado en el tiempo que la amilasa.
Punción peritoneal no es un método ideal.
Radiografía de tórax: Efusión pleural, atelectasias basales izquierdas, elevación del hemidiafragma izquierdo, Sd. de Distress Respiratorio del Adulto: liquido intersticial, diagnósticos diferenciales.
Radiografía abdominal: Asa centinela (asa yeyunal proximal dilatada en hemiabdomen superior proximal al lecho pancreático), aire en la “C” duodenal por íleo duodenal, Colon “cut-off”, borramiento de la sombra de los psoas, íleo, litiasis vesicular, calcificaciones pancreáticas.
TC helicoidal con doble contraste: El estudio ideal.
RM: No revela ventajas con respecto a la TC.
CPRE.
Otras Causas Hiperamilasemia:
- Enfermedades de las vías biliares.
- Obstrucción intestinal e Infarto Mesentérico.
- Apendicitis aguda y peritonitis.
- Ulcera péptica perforada.
- Embarazo ectópico roto.
- Salpingitis.
- Enfermedades de las glándulas salivales.
- Neumonía.
- TCE.
Diagnósticos Diferenciales:
- Estenosis Pilórica.
- Ulcera péptica perforada o penetrada.
- Isquemia intestinal.
- Obstrucción intestinal.
- Colecistitis aguda.
- Infarto de cara diafragmática del miocardio.
Evolución Clínica
90% tendrá una evolución autolimitada que requerirá medidas simples de tratamiento.
El 10% evolucionará a formas graves de la enfermedad (alta morbilidad y mortalidad) requiriendo medidas de soporte vital y cuidados intensivos.
Para identificar precozmente a este grupo existen indicadores predictivos de la severidad:
- Criterios de Ranson.
- Criterios de Glasgow.
- APACHE II. (Acute Physiology And Chronic Health Evaluation)
- Clasificación tomográfica de Balthazar.
Criterios de Ranson para la Pancreatitis no Biliar:
Al ingreso
1. EDAD >55 años.
2. GB > 16.000 / mm³.
3. GLICEMIA > 200 mg/L.
4. TGO > 250 UI/L.
5. LDH > 350 UI/L.
A las 48 horas
1. Caída de Hcto > 10 puntos.
2. Alza del BUN > de 5 mg/dl.
3. Calcemia < 8 mg/dl.
4. pO2 < 60 con FiO2 de 21%.
5. Déficit de base > - 4 mEq/L.
6. Secuestro de volumen > 6 L.
Número de criterios – mortalidad
0-2 -----------0,9%
3-4 ---------- 15%
5-6 -----------50%
7-11 ----------95%
Leucocitosis: SIRS, infección
Hiperglicemia: Hipoinsulinemia por lesión celular. Tono adrenérgico aumentado.
Caída del Hcto: Por hemorragia.
Alza del BUN: Por disminución del volumen circulante efectivo por formación de un tercer espacio.
Hipocalcemia: Por hipoalbuminemia funcional y por depósitos de calcio en focos de necrosis grasa.
Caída del PO2: Por Sd. De distress respiratorio del adulto.
Aumento del déficit de base: Por hipoperfusión e hipo-oxigenación tisular.
Secuestro de líquido: Por formación de un tercer espacio por aumento de la permeabilidad endotelial.
Criterios de Ranson para Pancreatitis Biliar:
Al ingreso
1. Edad > 70
2. GB > 18.000
3. Glicemia > 200
4. LDH > 400
5. TGO > 250
A las 48 horas
1. Caída del Hcto > 10
2. BUN > 2
3. Calcemia < 8
4. Déficit de base > -5
5. Secuestro de liquido > 4 L
6. pO2 < 60 con FiO2 de 21%
Criterios de Glasgow:
1. GB > 15.000 /mm³.
2. Glicemia >2 gr./L.
3. BUN > 16 mmol/L.
4. PO2 < 60 mm. Hg.
5. Calcio > 2.0 mmol/L.
6. Albúmina < 3.2 mg.%.
7. LDH > 600 U/L.
8. SGOT ó SGPT > 200 U/L.
3 o más factores a las 48 h. del ingreso denotan una pancreatitis severa.
Clasificación Tomográfica de Balthazar:
A ----- páncreas normal
B ----- edema pancreático focal o difuso
C ----- inflamación peripancreática
D ----- 1 colección peripancreática
E ----- 2 o más colecciones y/o gas peripancreático
A) Complicaciones Tempranas
- Shock.
- Falla renal.
- Falla pulmonar.
- Déficit nutricional.
- Hipocalcemia e hiperglicemia.
Shock: Edema peripancreático, tercer espacio, émesis, hemorragia.
Hipocalcemia e hiperglicemia: Corregirlas con calcio e insulina.
En la mayoría de los pacientes se reinicia la vía oral dentro de la primera semana de iniciado el cuadro. En aquellos en que no se puede se indica NPT tan pronto su condición hemodinámica y cardiopulmonar lo permitan. Si el paciente va a quirófano, un acceso enteral puede ser requerido (Yeyunostomia o sonda naso-yeyunal).
Falla pulmonar: Alguna complicación respiratoria se observa hasta en un 50% de los casos. La hipoxemia es muy frecuente en las primeras 48 h. La fosfolipasa A circulante producto de los fenómenos lipolíticos está aumentada lo que interfiere con el surfactante. Se puede observar elevación hemidiafragmática, efusión pleural, neumonía y edema pulmonar.
Infección y sepsis: Por traslocación bacteriana.
Falla renal: Por disminución del volumen circulante efectivo se puede producir una IRA prerrenal.
B) Complicaciones Mediatas
Infección Pancreática Secundaria:
- Esta complicación es responsable del 80% de las muertes.
- La traslocación bacteriana e infección por puntos de venoclisis son el punto de partida.
- Los gérmenes implicados son Gram (-) y anaerobios de la flora intestinal, Pseudomonas, Gram (+) y Candida.
1- Absceso pancreático.
2- Necrosis pancreática sobreinfectada.
El absceso pancreático es una colección intrabdominal bien circunscrita susceptible a ser drenada por vía percutánea.
La necrosis pancreática sobreinfectada se trata de áreas focales o difusas de parénquima pancreático no viable asociado a necrosis grasa peripancreática con infección asociada por bacterias u hongos. No se puede drenar por vía percutánea y el paciente debe ser operado para debridación y limpieza quirúrgica. Se puede manejar con drenajes o como un abdomen abierto. La tendencia es a hacer esto último.
Estas complicaciones se sospechan en el contesto de una pancreatitis severa (definida por la presencia de 3 o más criterios de Ranson) cuando se observa un franco deterioro clínico después de la primera semana de enfermedad y en pacientes con bacteriemia documentada. Persiste la hiperamilasemia, gas en retroperitoneo. Se puede hacer punción guiada por TAC para obtener muestra para Gram y cultivo.
C) Complicaciones Tardías
Pseudoquiste Pancreático:
- Se observa típicamente a las 4 semanas de iniciada la pancreatitis.
- Más frecuente en pancreatitis por alcohol (65%).
- Persistencia o recurrencia del dolor, nauseas y vómitos, en ocasiones masa palpable.
- Hiperamilasemia.
- Se forma por la disrupción de un ducto pancreático con la consiguiente extravasación de jugo pancreático y su colección intrabdominal enmarcada por las vísceras que rodean al páncreas.
- Su persistencia se debe a la persistencia de la disrupción del ducto ya que la cicatrización del ducto lleva a la reabsorción y desaparición del pseudoquiste de manera espontánea. Por tanto se espera de 4 a 6 semanas antes de decidir cualquier otro tratamiento a menos que se complique y que la clínica así lo permita. El diagnostico se hace con TC y el seguimiento con US abdominal.
- Las variedades de tratamiento son: Drenaje quirúrgico interno (la técnica que se prefiere es la cisto-yeyuno anastomosis), Drenaje quirúrgico externo, Drenaje percutáneo, CPRE.
- Complicaciones del pseudoquíste pancreático:
a) Infección. 10% de los casos. El manejo es drenaje percutáneo
b) Obstrucción. Gástrica, duodenal, yeyunal, inclusive, del sistema portal.
c) Hemorragia. Por erosión de vasos de vísceras vecinas. Grave.
d) Ruptura. Abdomen agudo quirúrgico.
PANCREATITIS CRÓNICA
Concepto:
Enfermedad inflamatoria crónica que afecta a la glándula caracterizada por cambios anatómicos y funcionales irreversibles. Son típicos:
- Episodios recurrentes o persistentes de dolor abdominal.
- Insuficiencia pancreática exocrina.
- Dilatación del sistema ductal.
- Fibrosis y calcificación de la glándula.
- Puede ser focal, segmental o difusa.
- Principal etiología: El alcohol (75%).
Otras causas son: Estenosis congénitas y adquiridas del ducto pancreático, post-traumáticas, Fibrosis quística, Pancreas Divisum, Pancreatitis familiar, estados crónicos de hipercalcemia.
Cuadro Clínico
- Dolor abdominal en epigastrio, irradiado en banda a la espalda. Recurrente o persistente. - Insuficiencia pancreática exocrina
- Síndrome de mala absorción. Diarrea y esteatorrea.
- Pérdida de peso.
- Diabetes secundaria.
A medida que empeora la enfermedad, los periodos de acalmia son menores y los periodos de dolor, son mayores. El empeoramiento del dolor después de la ingesta de alimentos y alcohol es típico de la pancreatitis crónica.
Diagnóstico
1.- Hiperamilasemia y leucocitosis en las exacerbaciones agudas.
2.- Grasa fecal y curva de tolerancia a la glucosa para evaluar función exocrina y endocrina.
3.- TC abdominal.
- Dilatación ductal.
- Calcificaciones pancreáticas.
- Densidad heterogénea del parénquima.
- Lesiones quísticas.
4.- CPRE.
Complicaciones:
- Obstrucción del Colédoco distal (diferenciar de obstrucción maligna).
- Obstrucción duodenal.
- Fístulas Pancreáticas.
- Ascitis pancreática crónica.
- Efusión pleural pancreática.
- Fístulas pancreático - entéricas.
- Trombosis de la vena esplénica.
Si la disrupción ductal ocurre en el contexto de una pancreatitis aguda o una reagudización de una pancreatitis crónica los tejidos inflamados colectan el jugo pancreático y se forma un pseudoquiste. Si esta disrupción ocurre sin un proceso inflamatorio peripancreático el liquido difundirá y si el ducto es anterior se formara una ascitis pancreática o si el ducto es posterior (vía retroperitoneo, mediastino posterior, cavidad pleural) se formara una efusión pleural.
El manejo es conservador: NPT, drenaje. Si no responde en 6 semanas el tratamiento quirúrgico se impone.
La fístula pancreático-enterica es por el drenaje espontáneo de un absceso pancreático a una víscera hueca. Siempre son quirúrgicas. Son raras.
Pancreatitis es la causa del 65% de las trombosis de la vena esplénica. Puede ser silente o manifestarse como HTP con varices esofágicas. El tratamiento es la esplenectomia.
Tratamiento:
A.- Médico
- Suprimir ingestión alcohólica.
- Tratar la diabetes.
- Terapia con enzimas pancreáticas.
- Analgésicos.
- Soporte nutricional.
B.- Quirúrgico
- En el dolor intratable.
Clase creada por el Dr. Carlos Bellorin.